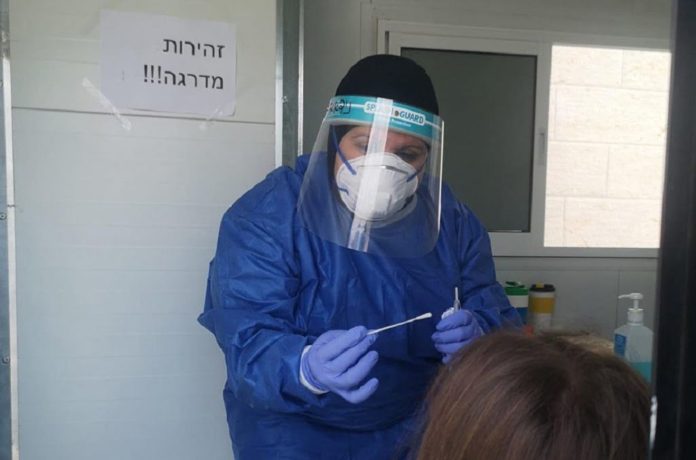
C’est un succès pour le traitement aux anticorps Covid-19 israélien. 11 des 12 patients de l’essai traités avec le traitement IgG Covid-19 de Kamada en Israël se sont rétablis et sont sortis de l’hôpital.
La société biopharmaceutique israélienne Kamada a annoncé cette semaine que les premiers résultats provisoires d’un essai clinique impliquant son traitement par anticorps dérivés du plasma contre le COVID-19 montrent un taux d’amélioration de plus de 90% chez les patients.
L’essai clinique multicentrique de phase 1/2 de la société a été lancé le mois dernier pour évaluer l’innocuité, la pharmacocinétique et la pharmacodynamie du produit d’immunoglobuline hyperimmunoglobuline (IgG) dérivée du plasma de Kamada en tant que traitement potentiel pour les patients atteints de COVID-19 atteints de pneumonie qui sont hospitalisés mais non ventilé.
Les résultats intermédiaires ont montré que les symptômes se sont améliorés chez 11 patients sur 12 dans les 24 à 48 heures suivant le traitement, soit un taux de plus de 91%. Les 11 patients sont ensuite sortis de l’hôpital dans un délai médian de 4,5 jours après avoir reçu le traitement, a rapporté Kamada.
Les 12 patients éligibles (âgés de 34 à 69 ans) ont reçu le traitement aux anticorps à une dose unique de 4 grammes dans les cinq à 10 jours suivant les premiers symptômes. Des suivis auront lieu pendant 84 jours après le traitement.
À ce jour, cinq des 12 patients ont terminé un suivi post-traitement de 21 jours, deux patients ont suivi un suivi post-traitement de 14 jours et cinq autres patients ont terminé un suivi post-traitement de sept jours.
L’état de santé d’un patient, qui a terminé le suivi post-traitement de 14 jours, s’est détérioré et ce patient est actuellement sous ventilation mécanique, a déclaré Kamada. Un autre patient a eu un événement indésirable grave quatre jours après avoir reçu le traitement, un événement qui a été classé comme non lié au traitement que le patient a reçu dans l’essai.
«Le profil d’innocuité de notre produit IgG et l’amélioration des symptômes préalablement démontrée par ces résultats sont favorables et nous prévoyons de continuer à caractériser l’activité de neutralisation virale du produit afin d’étalonner la dose de traitement», a déclaré le Dr Naveh Tov, vice-président du développement clinique de Kamada et directeur médical, dans un communiqué.
Les résultats définitifs des essais sont attendus d’ici janvier 2021, a indiqué la société.
«Le plasma de convalescence joue un rôle important dans la réponse immédiate et intermédiaire à la maladie», a déclaré le PDG de Kamada, Amir London, dans le communiqué.
«Le produit IgG dérivé du plasma, tel que développé par Kamada, est considéré comme présentant de multiples avantages par rapport à la transfusion plasmatique de convalescence, tels que des niveaux d’anticorps normalisés, une puissance plus élevée, un traitement d’inactivation virale étendu, l’absence d’exigence de correspondance de type sanguin, des volumes de perfusion plus petits , la possibilité d’être produit en grandes quantités, une durée de conservation plus longue attendue et des conditions de stockage préférées », a-t-il ajouté.